《物理化学》期末机考
1.[单选题] 科尔劳施定律认为电解质溶液的摩尔电导率与其浓度呈线性关系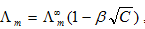 ,这一规律是用于()。
,这一规律是用于()。
A.弱电解质
B.强电解质的稀溶液
C.无限稀溶液
D.摩尔浓度为1的溶液
答:————
2.[单选题] 某反应A→B+C,当A的浓度增加一倍时,反应的半衰期t1/2也增加一倍时,则此反应的级数为()。
A.零级
B.一级
C.无法判断
D.二级
答:————
3.[单选题] 银锌电池 则该电池的标准电动势
则该电池的标准电动势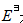 是()。
是()。
A.1.180 V
B.1.560 V
C.0.038 V
D.2.359 V
答:————
4.[单选题] CaCl2的摩尔电导率与其离子的摩尔电导率的关系是()。
A.∧m∞(CaCl2)=2[λm∞(Ca2+)+λm∞(Cl-)]
B.∧m∞(CaCl2)=λm∞(Ca2+)+λm∞(Cl-)
C.∧m∞(CaCl2)=λm∞(Ca2+)+2λm∞(Cl-)
D.∧m∞(CaCl2)=1/2λm∞(Ca2+)+λm∞(Cl-)
答:————
5.[单选题] 在25℃时,A和B两种气体在同一溶剂中的享利系数分别为kA和kB,且kA=2kB,当A和B压力相同时,在该溶液中A和B的浓度之间的关系为: ()。
A.cA = cB
B.2cA = cB
C.不确定
D.cA =2cB
答:————
6.[单选题] 热力学第一定律ΔU=Q+W 只适用于()。
A.相变化
B.化学变化
C.单纯状态变化
D.封闭物系的任何变化
答:————
7.[单选题] 热力学第三定律可以表示为()。
A.在0K时,任何完整晶体的熵等于零
B.在0K时,任何晶体的熵等于零
C.在0℃时,任何晶体的熵等于零
D.在0℃时,任何完整晶体的熵等于零
答:————
8.[单选题] 若向摩尔电导率为1.4×10-2s×m2×mol-1的CuSO4溶液中,加入1m3的纯水,这时CuSO4摩尔电导率为()。
A.不变;
B.降低;
C.增高;
D.不能确定
答:————
9.[单选题] 对于恒沸混合物,下列说法错误的是()。
A.与化合物一样具有确定组成
B.平衡时气相和液相组成相同
C.不具有确定组成
D.其沸点随外压的改变而改变
答:————
10.[单选题] 在α,β两相中均含有A和B两种物质,当达到平衡时,下列种哪情况是正确的:()。
A.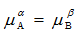
B.
C.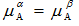
D.
答:————
11.[单选题] 系统经不可逆循环过程,则有()。
A.ΔS系统 = 0,ΔS环<0
B.ΔS系统 = 0,ΔS隔>0
C.ΔS系统 = 0,ΔS隔<0
D.ΔS系统>0,ΔS隔>0
答:————
12.[单选题] 质量作用定律适用于()。
A.连串反应
B.基元反应
C.平行反应
D.对峙反应
答:————
13.[单选题] 0.3 mol.kg-1Na2SO4水溶液的离子强度是()。
A.0.3
B.1.2
C.0.9
D.1.8
答:————
14.[单选题] 对于理想气体,下列关系中哪个是不正确的()。
A.
B.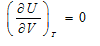
C.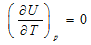
D.
答:————
15.[单选题] 某一电池反应,若算得其电池电动势为负值时,表示此电池反应是()。
A.正向进行
B.不可能进行
C.反应方向不确定
D.逆向进行
答:————
16.[单选题] 下列说法不属于可逆电池特性的是()。
A.电池所对应的化学反应ΔrGm = 0
B.电池内的化学反应在正逆方向彼此相反;
C.电池放电与充电过程电流无限小;
D.电池的工作过程肯定为热力学可逆过程;
答:————
17.[单选题] 对于理想溶液,混合过程的热力学函数的变化为()。
A.ΔmixH=0,ΔmixS=0,ΔmixG<0
B.ΔmixV=0,ΔmixS=0,ΔmixH=0
C.ΔmixH=0,ΔmixG=0,ΔmixS>0
D.ΔmixV=0,ΔmixH=0,ΔmixS>0
答:————
18.[单选题] nsi-language:EN-US;areast-language:ZH-CN;idi-language:AR-SA">. areast-font-family:华文中宋;color:#003300;nsi-language:EN-US;areast-language:
ZH-CN;idi-language:AR-SA;idi-font-weight:bold"> areast-font-family:宋体;ont-kerning:1.0pt;nsi-language:EN-US;
areast-language:ZH-CN;idi-language:AR-SA;idi-font-weight:bold">CaCO3(s)部分分解为 nsi-language:EN-US;areast-language:ZH-CN;idi-language:AR-SA;
idi-font-weight:bold">CO2和 nsi-language:EN-US;areast-language:ZH-CN;idi-language:AR-SA;
idi-font-weight:bold">CaO(s),达平衡时体系的相数与组分数为()。
A.3, 3
B.3, 2
C.2, 2
D.3, 1
答:————
19.[单选题] 如图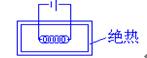 ,在绝热盛水容器中,浸入电阻丝,通电一段时间,通电后水及电阻丝的温度均略有升高,今以电阻丝为体系有()。
,在绝热盛水容器中,浸入电阻丝,通电一段时间,通电后水及电阻丝的温度均略有升高,今以电阻丝为体系有()。
A.W <0,Q <0,U >0
B.W>0,Q <0,U >0
C.W <0,Q =0,U >0
D.W =0,Q <0,U <0
答:————
20.[单选题] 下列既是偏摩尔量又是化学势的是()。
A.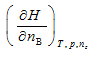
B.
C.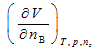
D.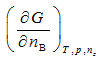
答:————
21.[问答题] 写出下列定律或方程的数学表达式,用简单的一句话说明其主要应用或要解决什么问题?(1)热力学第一定律;第二定律;第三定律。(2)化学反应的恒温方程。(3)相律。
答:————
22.[问答题] 甲酸在金表面发生分解反应的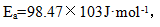 并测得413K时反应的速率常数为
并测得413K时反应的速率常数为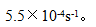 。求:若使反应在1小时转化90%所需控制的反应温度T。
。求:若使反应在1小时转化90%所需控制的反应温度T。
答:————
23.[问答题] 强电解质MX、Y和HY的摩尔极限电导分别为L1.L2.L3,则HX的摩尔极限电导为(? )。
答:————
24.[问答题] 反应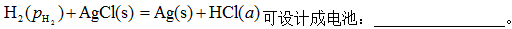
答:————
25.[问答题] 绝热可逆过程的ΔS(? )0,绝热不可逆压缩过程的ΔS (? )0。
答:————
26.[问答题] 反应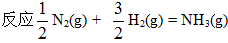 , 当H2因反应消耗了0.3mol 时,反应进度ξ= (? )。
, 当H2因反应消耗了0.3mol 时,反应进度ξ= (? )。
答:————
27.[问答题] 在一定温度下, ,由纯液态物质A和B形成理想液态混合物,当气—液两相达到平衡时,气相的组成
,由纯液态物质A和B形成理想液态混合物,当气—液两相达到平衡时,气相的组成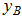 与液相组成
与液相组成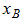 的关系为
的关系为 。
。
答:————
28.[问答题] 具有简单级数的反应,速率常数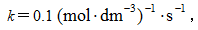 反应的起始浓度
反应的起始浓度 ,则反应级数n=(? ),半衰期t1/2=(? )s。
,则反应级数n=(? ),半衰期t1/2=(? )s。
答:————
29.[问答题] 在 溶液中加入10 cm3水,其电导率将(? ),摩尔电导率将(? )(填入增加、减小、不能确定)。
溶液中加入10 cm3水,其电导率将(? ),摩尔电导率将(? )(填入增加、减小、不能确定)。
答:————
30.[问答题] 公式上联系热力学和电化学的主要桥梁,该公式的应用条件是(? )。
公式上联系热力学和电化学的主要桥梁,该公式的应用条件是(? )。
答:————
1.[单选题] 科尔劳施定律认为电解质溶液的摩尔电导率与其浓度呈线性关系
A.弱电解质
B.强电解质的稀溶液
C.无限稀溶液
D.摩尔浓度为1的溶液
答:————
2.[单选题] 某反应A→B+C,当A的浓度增加一倍时,反应的半衰期t1/2也增加一倍时,则此反应的级数为()。
A.零级
B.一级
C.无法判断
D.二级
答:————
3.[单选题] 银锌电池
A.1.180 V
B.1.560 V
C.0.038 V
D.2.359 V
答:————
4.[单选题] CaCl2的摩尔电导率与其离子的摩尔电导率的关系是()。
A.∧m∞(CaCl2)=2[λm∞(Ca2+)+λm∞(Cl-)]
B.∧m∞(CaCl2)=λm∞(Ca2+)+λm∞(Cl-)
C.∧m∞(CaCl2)=λm∞(Ca2+)+2λm∞(Cl-)
D.∧m∞(CaCl2)=1/2λm∞(Ca2+)+λm∞(Cl-)
答:————
5.[单选题] 在25℃时,A和B两种气体在同一溶剂中的享利系数分别为kA和kB,且kA=2kB,当A和B压力相同时,在该溶液中A和B的浓度之间的关系为: ()。
A.cA = cB
B.2cA = cB
C.不确定
D.cA =2cB
答:————
6.[单选题] 热力学第一定律ΔU=Q+W 只适用于()。
A.相变化
B.化学变化
C.单纯状态变化
D.封闭物系的任何变化
答:————
7.[单选题] 热力学第三定律可以表示为()。
A.在0K时,任何完整晶体的熵等于零
B.在0K时,任何晶体的熵等于零
C.在0℃时,任何晶体的熵等于零
D.在0℃时,任何完整晶体的熵等于零
答:————
8.[单选题] 若向摩尔电导率为1.4×10-2s×m2×mol-1的CuSO4溶液中,加入1m3的纯水,这时CuSO4摩尔电导率为()。
A.不变;
B.降低;
C.增高;
D.不能确定
答:————
9.[单选题] 对于恒沸混合物,下列说法错误的是()。
A.与化合物一样具有确定组成
B.平衡时气相和液相组成相同
C.不具有确定组成
D.其沸点随外压的改变而改变
答:————
10.[单选题] 在α,β两相中均含有A和B两种物质,当达到平衡时,下列种哪情况是正确的:()。
A.
B.
C.
D.
答:————
11.[单选题] 系统经不可逆循环过程,则有()。
A.ΔS系统 = 0,ΔS环<0
B.ΔS系统 = 0,ΔS隔>0
C.ΔS系统 = 0,ΔS隔<0
D.ΔS系统>0,ΔS隔>0
答:————
12.[单选题] 质量作用定律适用于()。
A.连串反应
B.基元反应
C.平行反应
D.对峙反应
答:————
13.[单选题] 0.3 mol.kg-1Na2SO4水溶液的离子强度是()。
A.0.3
B.1.2
C.0.9
D.1.8
答:————
14.[单选题] 对于理想气体,下列关系中哪个是不正确的()。
A.
B.
C.
D.
答:————
15.[单选题] 某一电池反应,若算得其电池电动势为负值时,表示此电池反应是()。
A.正向进行
B.不可能进行
C.反应方向不确定
D.逆向进行
答:————
16.[单选题] 下列说法不属于可逆电池特性的是()。
A.电池所对应的化学反应ΔrGm = 0
B.电池内的化学反应在正逆方向彼此相反;
C.电池放电与充电过程电流无限小;
D.电池的工作过程肯定为热力学可逆过程;
答:————
17.[单选题] 对于理想溶液,混合过程的热力学函数的变化为()。
A.ΔmixH=0,ΔmixS=0,ΔmixG<0
B.ΔmixV=0,ΔmixS=0,ΔmixH=0
C.ΔmixH=0,ΔmixG=0,ΔmixS>0
D.ΔmixV=0,ΔmixH=0,ΔmixS>0
答:————
18.[单选题] nsi-language:EN-US;areast-language:ZH-CN;idi-language:AR-SA">. areast-font-family:华文中宋;color:#003300;nsi-language:EN-US;areast-language:
ZH-CN;idi-language:AR-SA;idi-font-weight:bold"> areast-font-family:宋体;ont-kerning:1.0pt;nsi-language:EN-US;
areast-language:ZH-CN;idi-language:AR-SA;idi-font-weight:bold">CaCO3(s)部分分解为 nsi-language:EN-US;areast-language:ZH-CN;idi-language:AR-SA;
idi-font-weight:bold">CO2和 nsi-language:EN-US;areast-language:ZH-CN;idi-language:AR-SA;
idi-font-weight:bold">CaO(s),达平衡时体系的相数与组分数为()。
A.3, 3
B.3, 2
C.2, 2
D.3, 1
答:————
19.[单选题] 如图
 ,在绝热盛水容器中,浸入电阻丝,通电一段时间,通电后水及电阻丝的温度均略有升高,今以电阻丝为体系有()。
,在绝热盛水容器中,浸入电阻丝,通电一段时间,通电后水及电阻丝的温度均略有升高,今以电阻丝为体系有()。A.W <0,Q <0,U >0
B.W>0,Q <0,U >0
C.W <0,Q =0,U >0
D.W =0,Q <0,U <0
答:————
20.[单选题] 下列既是偏摩尔量又是化学势的是()。
A.
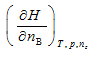
B.

C.
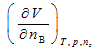
D.
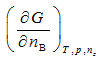
答:————
21.[问答题] 写出下列定律或方程的数学表达式,用简单的一句话说明其主要应用或要解决什么问题?(1)热力学第一定律;第二定律;第三定律。(2)化学反应的恒温方程。(3)相律。
答:————
22.[问答题] 甲酸在金表面发生分解反应的
答:————
23.[问答题] 强电解质MX、Y和HY的摩尔极限电导分别为L1.L2.L3,则HX的摩尔极限电导为(? )。
答:————
24.[问答题] 反应
答:————
25.[问答题] 绝热可逆过程的ΔS(? )0,绝热不可逆压缩过程的ΔS (? )0。
答:————
26.[问答题] 反应
答:————
27.[问答题] 在一定温度下,
答:————
28.[问答题] 具有简单级数的反应,速率常数
答:————
29.[问答题] 在
答:————
30.[问答题]
答:————
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
