一定温度下,在一个10 L密闭容器中发生某可逆反应,其平衡常数表达式为K=<img alt="1" src="/tk/20210511/1620748544206.
一定温度下,在一个10 L密闭容器中发生某可逆反应,其平衡常数表达式为K=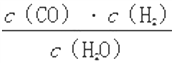 。请回答下列问题。
。请回答下列问题。
(1)若温度升高,K增大,则该反应是________反应(填“吸热”或“放热”)。
(2)能判断该反应一定达到平衡状态的是________(填字母序号)。
A.v正(H2O)=v逆(H2)
B.容器中气体的平均相对分子质量不随时间改变
C.消耗n mol H2的同时消耗n mol CO
D.容器中物质的总物质的量不随时间改变
【答案】吸热 AB
【解析】(1)温度升高,K增大,说明平衡正向移动,因此正反应为吸热反应,故答案为:吸热;
(2)根据平衡常数的定义,生成物浓度的幂之积与反应物浓度的幂之积之比为平衡常数,反应的方程式为C(s)+H2O(g)⇌CO(g)+H2 (g)。A、υ正(H2O)=υ逆(H2)时,正逆反应速率相同,反应达到平衡,故A正确;B、反应前后气体的物质的量不相同,气体质量变化,容器中气体的平均相对分子质量不随时间变化即达到平衡,故B正确;C、消耗nmolH2的同时消耗nmolCO,反应都代表逆反应,不能说明反应达到平衡状态,故C错误;D、容器中物质的总物质的量始终不变,故D错误;故答案为:AB。
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
