实验室制备1,2﹣二溴乙烷的反应原理如下: CH3CH2OH <img alt="1" src="/tk/20210511/1620748261876.png&qu
实验室制备1,2﹣二溴乙烷的反应原理如下: CH3CH2OH 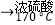 CH2═CH2CH2═CH2+Br2→BrCH2CH2Br可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图所示:
CH2═CH2CH2═CH2+Br2→BrCH2CH2Br可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图所示: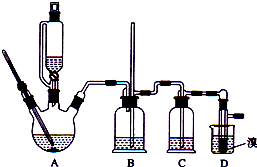 有关数据列表如下:
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g•cm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | ﹣1l6 |
回答下列问题:(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是______;(填正确选项前的字母) a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成(2)在装置C中应加入______ , 其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母) a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液(3)判断该制备反应已经结束的最简单方法是______;(4)将1,2﹣二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在______层(填“上”、“下”);(5)若产物中有少量未反应的Br2 , 最好用______洗涤除去;(填正确选项前的字母) a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇(6)若产物中有少量副产物乙醚.可用______的方法除去;(7)反应过程中应用冷水冷却装置D,其主要目的是______;但又不能过度冷却(如用冰水),其原因是______
【答案】(1)d
(2)c
(3)溴的颜色完全褪去
(4)下
(5)b
(6)蒸馏
(7)避免溴的大量挥发;产品1,2﹣二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管
【解析】解:(1.)乙醇在浓硫酸140℃的条件下,发生分子内脱水,生成乙醚,所以在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是减少副产物乙醚生成,故d正确, 所以答案是:d;
(2.)浓硫酸具有强氧化性,将乙醇氧化成二氧化碳,自身被还原成二氧化硫,二氧化碳、二氧化硫能和氢氧化钠溶液反应,所以装置C中为氢氧化钠溶液,
所以答案是:c;
(3.)乙烯和溴水发生加成反应生成1,2﹣二溴乙烷,1,2﹣二溴乙烷为无色,则溴的颜色完全褪去时,该制备反应已经结束,
所以答案是:溴的颜色完全褪去;
(4.)1,2﹣二溴乙烷和水不互溶,1,2﹣二溴乙烷密度比水大,所以振荡后静置后产物应在分液漏斗的下层,
所以答案是:下;
(5.)常温下Br2和氢氧化钠发生反应:2NaOH+Br2═NaBr+NaBrO+H2O,
所以答案是:b;
(6.)1,2﹣二溴乙烷与乙醚的沸点不同,两者均为有机物,互溶,需要用蒸馏的方法将它们分离,
所以答案是:蒸馏;
(7.)溴在常温下,易挥发,乙烯与溴反应时放热,溴更易挥发,冷却可避免溴的大量挥发,但1,2﹣二溴乙烷的凝固点9℃较低,不能过度冷却,否则会凝固而堵塞导管,
所以答案是:避免溴的大量挥发;产品1,2﹣二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
