2.3gNa在干燥的空气中长时间放置,得到Na的氧化物3.5g试确定该氧化物的组成为_____________,它们的质量分别为_____________若将此氧化物投入足量水中,可得O2______
2.3gNa在干燥的空气中长时间放置,得到Na的氧化物3.5g试确定该氧化物的组成为_____________,它们的质量分别为_____________若将此氧化物投入足量水中,可得O2__________g
【答案】Na2O、Na2O2;1.55g、1.95g;0.4g
【解析】设混合物中氧化钠和过氧化钠的物质的量分别是xmol、ymol,则2x+2y=2.3÷23=0.1,62x+78y=3.5,解得x=0.025,y=0.025,因此氧化钠和过氧化钠的质量分别是0.025mol×62g/mol=1.55g,0.025mol×78g/mol=1.95g;氧化钠和水生成氢氧化钠,过氧化钠和水反应生成氢氧化钠和氧气,根据方程式2Na2O2+2H2O=4NaOH+O2↑可知生成氧气的质量是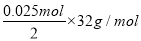 =0.4g。
=0.4g。
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
