某课外小组设计的实验室制取乙酸乙酯的装置如图1: 己知:A中放有浓硫酸;B中放有乙醇、无水碳酸钠;D中放有饱和碳酸钠溶液.<br/>有关有机物的沸点.
某课外小组设计的实验室制取乙酸乙酯的装置如图1: 己知:A中放有浓硫酸;B中放有乙醇、无水碳酸钠;D中放有饱和碳酸钠溶液.有关有机物的沸点.
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:(1)浓硫酸的作用:催化剂和______;反应中加入过量的乙醇,目的是______ .(2)仪器C的名称是______ , 其作用有冷凝乙酸乙酯和______ , 若反应前向D中加入几滴酚酞,溶液呈红色.实验完毕后,将烧杯D中的溶液充分振荡、静止,现象为______ .(3)若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:______ .(4)现拟分离乙酸乙酯(含少量乙醇和乙酸)粗产品,如图2是分离操作步骤流程图: 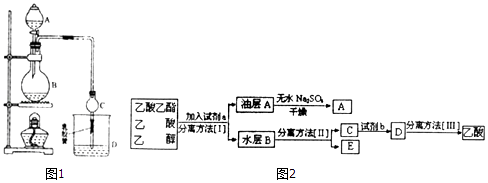 则试剂a是:______ , 试剂b是:______ . 分离方法I是______ , 分离方法II是______(5)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯,在未用指示剂的情况下,他们都先加NaOH溶液中和酯中过量的酸,然后用蒸馏水将酯分离出来.甲、乙两人实验结果如下:甲得到了显酸性的酯的混合物;乙得到了大量水溶性的物质;丙同学分析了上述实验目标产物后认为甲、乙的实验没有成功. 试解答下列问题:①甲实验失败的原因是:______ . ②乙实验失败的原因是:______ .
则试剂a是:______ , 试剂b是:______ . 分离方法I是______ , 分离方法II是______(5)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯,在未用指示剂的情况下,他们都先加NaOH溶液中和酯中过量的酸,然后用蒸馏水将酯分离出来.甲、乙两人实验结果如下:甲得到了显酸性的酯的混合物;乙得到了大量水溶性的物质;丙同学分析了上述实验目标产物后认为甲、乙的实验没有成功. 试解答下列问题:①甲实验失败的原因是:______ . ②乙实验失败的原因是:______ .
(1)吸水剂;提高乙酸的转化率
(2)球形干燥管;防止倒吸;红色变浅(或褪去)且出现分层现象
(3)CH3COOH+CH3CH218OH 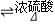 CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O
(4)饱和Na2CO3溶液;硫酸;分液;蒸馏
(5)所加的NaOH溶液较少,没有将余酸中和;所加的NaOH溶液过量使酯完全水解
【解析】解:(1)乙酸与乙醇需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,反应中加入过量乙醇的目的是提高乙酸的转化率(或提高乙酸乙酯的产率), 所以答案是:吸水剂;提高乙酸的转化率;(2)仪器C具有球形特征,为球形干燥管,乙酸、乙醇易溶于碳酸钠溶液,会导致装置内气体减小,容易发生倒吸,球形干燥管的管口伸入液面下可能发生倒吸,但球形干燥管体积大,可冷凝乙酸乙酯,也可以防止倒吸,碳酸钠为强碱弱酸盐,水解生成碳酸氢根离子和氢氧根离子,离子方程式:CO32﹣+H2O⇌HCO3﹣+OH﹣;碳酸钠溶液显碱性,遇到酚酞变红,实验完毕后,将烧杯D中的溶液充分振荡、静止,乙酸和碳酸钠反应而使溶液红色变浅,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,溶液分层,上层无色油体液体,
所以答案是:球形干燥管;防止倒吸;红色变浅(或褪去)且出现分层现象;(3)羧酸与醇发生的酯化反应中,羧酸中的羧基提供﹣OH,醇中的﹣OH提供﹣H,相互结合生成水,其它基团相互结合生成酯,同时该反应可逆,反应的化学方程式为CH3COOH+CH3CH218OH 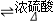 CH3CO18OC2H5+H2O,
CH3CO18OC2H5+H2O,
所以答案是:CH3COOH+CH3CH218OH 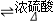 CH3CO18OC2H5+H2O;(4)由分离流程可知,加试剂a为碳酸钠,分离方法I为分液,油层含乙酸乙酯和水,加无水硫酸钠可吸收水,A为乙酸乙酯;水层含乙醇、乙酸钠、碳酸钠,分离方法II为蒸馏,E为乙醇,C中含乙酸钠、碳酸钠,加试剂b为硫酸,分离方法Ⅲ为蒸馏,
CH3CO18OC2H5+H2O;(4)由分离流程可知,加试剂a为碳酸钠,分离方法I为分液,油层含乙酸乙酯和水,加无水硫酸钠可吸收水,A为乙酸乙酯;水层含乙醇、乙酸钠、碳酸钠,分离方法II为蒸馏,E为乙醇,C中含乙酸钠、碳酸钠,加试剂b为硫酸,分离方法Ⅲ为蒸馏,
由上述分析可知a为饱和Na2CO3溶液,I为分液,II为蒸馏,b为硫酸,
所以答案是:饱和Na2CO3溶液;硫酸;分液;蒸馏;(5)①甲得到显酸性的酯的混合物,酸有剩余,说明是所加NaOH溶液不足未将酸完全反应,
所以答案是:所加的NaOH溶液较少,没有将余酸中和;②乙得到大量水溶性物质,说明没有酯,是因为所加NaOH溶液过量,酯发生水解,
所以答案是:所加的NaOH溶液过量使酯完全水解.
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
