用0.1032mol•L﹣1 HCl溶液滴定未知浓度的NaOH溶液,<br/>(1)某同学按下列步骤进行实验:①取一锥形瓶,用待测NaOH溶液润洗两次; ②在锥形瓶中加入25.00 mL待
用0.1032mol•L﹣1 HCl溶液滴定未知浓度的NaOH溶液,(1)某同学按下列步骤进行实验:①取一锥形瓶,用待测NaOH溶液润洗两次; ②在锥形瓶中加入25.00 mL待测NaOH溶液;③加入几滴石蕊试剂做指示剂;④取一支酸式滴定管,洗涤干净; ⑤直接往酸式滴定管中注入标准酸溶液,进行滴定; ⑥两眼注视着滴定管内盐酸溶液液面下降,直至滴定终点. 其中所述操作有错误的序号为______(2)取用25.00 mL待测NaOH溶液应用以下______(选填:“甲”、“乙”)装置,若取用NaOH溶液开始平视读数、结束时俯视读数,会导致所测氢氧化钠溶液浓度______(填“偏大““偏小“或“不变“)
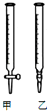 (3)若滴定开始前滴定管尖嘴中有一气泡,滴定结束后气泡消失, 则会导致所测氢氧化钠溶液浓度______(填“偏大““偏小“或“不变“)(4)若平行实验三次,记录的数据如下表
(3)若滴定开始前滴定管尖嘴中有一气泡,滴定结束后气泡消失, 则会导致所测氢氧化钠溶液浓度______(填“偏大““偏小“或“不变“)(4)若平行实验三次,记录的数据如下表
滴定次数 | 待测溶液的体积(/mL) | 标准HCl溶液的体积 | |
滴定前读数(/mL) | 滴定后读数(/mL) | ||
1 | 25.00 | 1.02 | 21.04 |
2 | 25.00 | 2.00 | 22.98 |
3 | 25.00 | 0.20 | 20.18 |
试计算待测NaOH溶液的物质的量浓度(列出计算过程).
【答案】(1)①③⑤⑥
(2)乙;偏大
(3)偏大
(4)解:三次滴定耗酸体积分别为20.02mL,20.98mL,19.98mL,其中第二次误差较大,取第一次与第三次平均值为20.00mL,c(NaOH)= 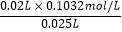 =0.08256mol/L;
=0.08256mol/L;
答:NaOH溶液的物质的量浓度为0.08256mol/L
【解析】解:(1)①锥形瓶装待测液时不能润洗,所以不能用待测NaOH溶液润锥形瓶,故①错误;②锥形瓶用于盛装一定体积的待测液,故②正确;③用石蕊作指示剂,变色不明显,故③错误;④取一支酸式滴定管,洗涤干净,故④正确;⑤酸式滴定管要用标准酸溶液润洗三次,不能直接往酸式滴定管中注入标准酸溶液,进行滴定,故⑤错误;⑥两眼应该注视着锥形瓶中溶液颜色变化,故⑥错误; 所以错误的有①③⑤⑥;
所以答案是:①③⑤⑥;(2)碱性溶液盛放在碱式滴定管中,图中甲为酸式滴定管,乙为碱式滴定管,所以盛放在乙中;取用NaOH溶液开始平视读数、结束时俯视读数,则体积偏大,滴定时消耗的标准溶液的体积偏大,所以所测氢氧化钠溶液浓度偏大;
所以答案是:乙;偏大;(3)若滴定开始前滴定管尖嘴中有一气泡,滴定结束后气泡消失,则消耗的标准溶液的体积偏大,由c(待测)= 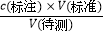 可知,所测氢氧化钠溶液浓度偏大;
可知,所测氢氧化钠溶液浓度偏大;
所以答案是:偏大;
【考点精析】关于本题考查的酸碱中和滴定,需要了解中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点才能得出正确答案.
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
