用下面的方法可以制得白色的Fe(OH)2沉淀.
(1)将实验所需的稀硫酸和氢氧化钠溶液加热煮沸,其目的是______ .
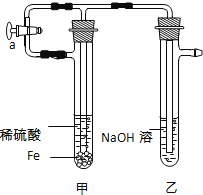
(2)按图所示连接好装置,打开止水夹a,反应片刻后,夹紧止水夹a,此时可观察到的现象是__________________ ;乙中发生反应的离子方程式是 ______ .
(3)将试管乙中的混合物倒入表面皿中,可观察到的现象________;反应的化学方程式是______ .
除去溶解在其中的氧;甲试管内导管中液面上升,流入乙中,乙试管中产生白色沉淀;Fe2++2OH﹣═Fe(OH)2;白色沉淀很快变成灰绿色,并逐渐加深,最后变成红褐色沉淀;4Fe(OH)2+O2+2H2O═4Fe(OH)3
【解析】(1)氢氧化亚铁不稳定,易被氧气氧化生成红褐色氢氧化铁沉淀,所以将实验所需的稀硫酸和氢氧化钠溶液加热煮沸,除去溶解在其中的氧,
所以答案是:除去溶解在其中的氧;
(2)甲中应预先盛放固态反应物铁屑,铁和稀硫酸反应生成硫酸亚铁和氢气,离子反应方程式为:Fe+2H+=Fe2++H2↑,打开止水夹a,反应片刻后,夹紧止水夹a,
导致甲装置中压强增大,甲试管内导管中液面上升,流入乙中,流入的溶液中含有硫酸亚铁,和氢氧化钠溶液反应,发生的离子反应方程式为:Fe2++2OH﹣=Fe(OH)2↓,因此乙中产生白色沉淀,
所以答案是:甲试管内导管中液面上升,流入乙中,乙试管中产生白色沉淀;Fe2++2OH﹣═Fe(OH)2;
(3)氢氧化亚铁不稳定,容易被空气中的氧气氧化,将试管乙中的混合物倒入表面皿中,可观察到:白色沉淀很快变成灰绿色,并逐渐加深,最后变成红褐色沉淀,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3 ,
所以答案是:白色沉淀很快变成灰绿色,并逐渐加深,最后变成红褐色沉淀;4Fe(OH)2+O2+2H2O═4Fe(OH)3;
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
