把1mol X和1mol Y混合于2L的密闭容器中,发生如下反应2X(g)+Y(g)=nZ(g)+2W(g),2min末X的物质的量为0.2mol,以Z的浓度表示的反应速率为0.1mol/(L•min
把1mol X和1mol Y混合于2L的密闭容器中,发生如下反应2X(g)+Y(g)=nZ(g)+2W(g),2min末X的物质的量为0.2mol,以Z的浓度表示的反应速率为0.1mol/(L•min)
请回答:
(1)前2min以X的浓度表示的平均反应速率
(2)n值.
【答案】(1)解:2min末X的物质的量为0.2mol,则v(X)=  =0.2mol/(L•min)
=0.2mol/(L•min)
答:前2min以X的浓度表示的平均反应速率为0.2mol/(L•min);
(2)解:速率之比等于其化学计量数之比,则n:2=0.1mol/(L•min):0.2mol/(L•min),故n=1,
答:n的值为1.
【解析】(1)根据v= 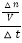 计算前2min以X的浓度表示的平均反应速率;(2)根据速率之比等于化学计量数之比计算n.
计算前2min以X的浓度表示的平均反应速率;(2)根据速率之比等于化学计量数之比计算n.
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
下一篇 :返回列表
