已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题
已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题:
(1)X元素原子基态时的电子排布式为__________,该元素的符号是_______;
(2)Y元素原子的价层电子的轨道表示式为_______,该元素的名称是_______;
(3)X与Z可形成化合物XZ3,该化合物的空间构型为__________;
(4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是____________________________________________;
(5)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由稳定性____________________、原因:____________________,沸点高低____________________、原因:____________________。
【答案】 1s22s22p63s23p63d104s24p3 As  氧 三角锥 As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O NH3>PH3>AsH3 因为键长越短,键能越大,化合物越稳定 NH3>AsH3>PH3 NH3可形成分子间氢键,沸点最高,AsH3相对分子质量比PH3大,分子键作用力大,因而AsH3比PH3沸点高
氧 三角锥 As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O NH3>PH3>AsH3 因为键长越短,键能越大,化合物越稳定 NH3>AsH3>PH3 NH3可形成分子间氢键,沸点最高,AsH3相对分子质量比PH3大,分子键作用力大,因而AsH3比PH3沸点高
(1)X原子4p轨道上有3个未成对电子,则其电子排布式为1s22s22p63s23p63d104s24p3,可推出其元素符号为As。
(2)Y原子最外层2p轨道上有2个未成对电子。可能是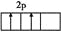 或
或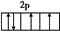 ,即Y可能为1s22s22p2或1s22s22p4,根据X2Y3,则Y只能是氧,Y元素原子的价层电子的轨道表示式为
,即Y可能为1s22s22p2或1s22s22p4,根据X2Y3,则Y只能是氧,Y元素原子的价层电子的轨道表示式为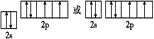 ,该元素的名称是氧。
,该元素的名称是氧。
(3)X、Y、Z原子序数之和为42,则Z的原子序数为42-33-8=1,Z是氢,化合物XZ3为AsH3,与NH3结构相似,为三角锥形。
(4)由题给信息可知As2O3与Zn和H2SO4反应生成AsH3、ZnSO4和H2O,根据电子守恒和原子守恒配平得As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O。
(5)稳定性:NH3>PH3>AsH3,因为键长越短,键能越大,化合物越稳定 沸点:NH3>AsH3>PH3,NH3可以形成分子间氢键,沸点最高;AsH3相对分子质量比PH3大,分子间作用力大,因而AsH3的沸点比PH3高。
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
